臭化銀 化学式と基本性質
臭化銀 化学式の構造と化学結合
臭化銀の化学式AgBrが示す構造は、塩化ナトリウム型の結晶構造であり、この結晶系は立方晶系に属しています。格子定数はa=5.768Åで、銀と臭素の原子間距離は2.88Åです。この構造は、1つの銀イオン(Ag⁺)が6個の臭素イオン(Br⁻)に囲まれ、逆に1つの臭素イオンが6個の銀イオンに囲まれる配位構造になっています。
臭化銀は主にイオン結合で成り立っており、銀が+1価の陽イオン、臭素が-1価の陰イオンとなって静電気力で結合しています。この結合は非常に強固であり、その結果として水にほとんど溶けない性質を持つようになります。溶解度積(Ksp)は4×10⁻¹³と非常に小さく、これは臭化銀が極めて難溶性の塩であることを示しています。
バンドギャップは2.5eVで、これは半導体としての性質を持つことを意味します。このバンドギャップ値が大きいほど光に対して敏感に反応し、この特性が写真感光材としての利用につながっています。
臭化銀 化学式の天然鉱物への現れ方
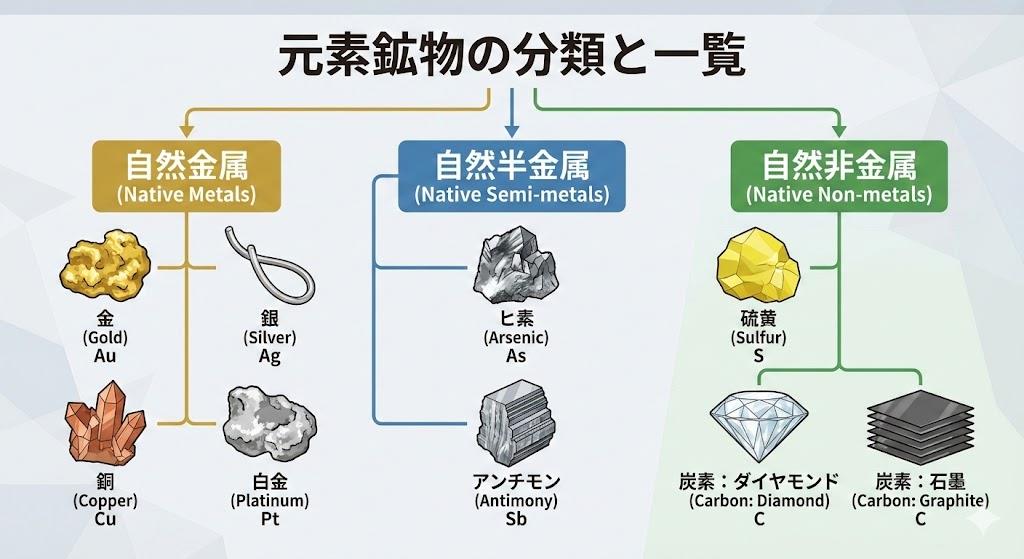
臭化銀は地球上に天然に存在する鉱物として「臭銀鉱」(ブロマルジライト、bromargyrite)として産出されます。臭銀鉱の化学式もAgBrで同じであり、主な産地はメキシコです。天然産の臭銀鉱は工業的に採掘される規模は限定的ですが、銀の副産物として回収されることがあります。
メキシコの鉱山では、銀を主成分とした鉱床の中に臭銀鉱が含まれており、銀資源の採掘過程で臭化銀が得られる場合もあります。これらの天然鉱物の化学分析によっても、化学式AgBrが確認されており、自然界でも人工的な化学反応と同じ化学式を持つ化合物が形成されていることが実証されています。
臭化銀 化学式からわかる製造方法
臭化銀は実験室やフィルム製造施設で合成されます。最も基本的な合成方法は、硝酸銀(AgNO₃)の水溶液に臭化物イオンを含む溶液を加えることです。化学反応式は以下の通りです。
Ag⁺(aq)+ Br⁻(aq)→ AgBr(s)
この反応では、硝酸銀水溶液に臭化カリウム(KBr)水溶液や臭化水素酸(HBr)を加えると、直ちに淡黄色の沈殿が生成されます。臭化銀の化学式に示されるように、銀イオン1個と臭化物イオン1個が結合して、1分子のAgBrが形成されるのです。
写真フィルム用の高品質な臭化銀結晶を製造する場合は、より複雑なプロセスが用いられます。ゼラチン等の保護コロイドを入れた水溶液中で、連続的に攪拌させながら、臭化カリウム水溶液と硝酸銀水溶液を同時に混入します。この製造方法では、流入速度をコントロールして「pAg」という水溶液中の銀イオン濃度プロファイルを維持することが極めて重要となります。
ゼラチン濃度が十分で銀イオン濃度が低い条件では、正八面体の結晶が得られます。最近では、双晶面を2つ以上含む平板粒子が特にフィルム用に多く使われており、この設計された粒子形状が感光性能に大きく影響します。
臭化銀 化学式と溶解性が決まる錯体形成
通常、臭化銀の化学式AgBrで表される化合物は水に不溶ですが、特定の試薬を加えると溶解する独特な性質を持っています。この現象は錯体形成によって起こります。
シアン化物イオンを加えた場合、以下のような反応が起こります。
AgBr + 2CN⁻ ⇌ [Ag(CN)₂]⁻ + Br⁻ (K = 1.2 × 10⁸)
チオ硫酸ナトリウム水溶液を加えた場合。
AgBr + 2S₂O₃²⁻ ⇌ [Ag(S₂O₃)₂]³⁻ + Br⁻ (K = 11)
濃アンモニア水を加えた場合。
AgBr + 2NH₃ ⇌ [Ag(NH₃)₂]⁺ + Br⁻ (K = 8 × 10⁻⁶)
これらの反応では、化学式に示されるAgBrの臭化銀が、配位結合によって銀イオンが他の分子に取り囲まれ、新しい錯イオンが形成されます。チオ硫酸ナトリウムによる反応は特に写真フィルムの定着処理で重要です。感光済みのフィルムをチオ硫酸ナトリウム定着液に浸すと、未反応の臭化銀が可溶性の錯体に変わり、フィルムから除去されます。
また、濃厚な臭化物の水溶液でも錯体を形成します。
AgBr + 3Br⁻ ⇌ [AgBr₄]³⁻ (K = 3 × 10⁻⁴)
この反応では、臭化物イオンが銀を取り囲んで配位することで、新しい錯体が形成されるのです。
臭化銀 化学式と光感応性の秘密
臭化銀の化学式AgBrで表される化合物が写真フィルムの感光材として使われるのは、この物質が独特な光感応性を持つためです。臭化銀は半導体であり、バンドギャップが2.5eVという値を持っています。
光が臭化銀に当たると、光のエネルギーが電子をバンドギャップを越えて励起させ、以下のような光化学反応が起こります。
2AgBr → 2Ag + Br₂
この反応では、化学式AgBrで表される臭化銀が分解され、銀原子と臭素が放出されます。この反応は複数回繰り返され、10~100個程度の銀原子が集まった「潜像核」(現像中心)が形成されます。潜像核は肉眼では見えませんが、現像処理によって増幅され、可視化されるのです。
フィルム写真の原理は以下の3段階からなっています。
1段階目の感光では、フィルムに光が当たると化学式AgBrの臭化銀が分解され始めます。感光乳剤中の臭化銀は粒径が極めて小さく、長径1μm未満が約60%、1~2μmが約30%という微粒子です。これらの微粒子が光を受けるので、極めて感度の高い感光材となっています。
2段階目の現像では、ヒドロキノンなどの還元剤に感光済みのフィルムを浸します。潜像核を中心にAgBrの還元が進み、銀の粒子がさらに成長します。この現像処理では、潜像核をもつ臭化銀粒子が還元され、全て銀に変わります。
3段階目の定着では、チオ硫酸ナトリウムを含む定着液を使用します。未反応の臭化銀が可溶性の錯イオンに変わり、フィルムから除去されます。
銀塩写真の周辺技術を考えると、この化学式AgBrで表される臭化銀なしには、デジタル化されるまでの長時間にわたって写真技術を支えてきた物質が存在しなかったことになります。
参考リンク:ウィキペディア「臭化銀」には、化学式、結晶構造、感光剤としての詳細なメカニズム、そして天然鉱物に関する情報が整理されています。
https://ja.wikipedia.org/wiki/%E8%87%AD%E5%8C%96%E9%8A%80
参考リンク:化学辞典の臭化銀の項目では、化学式、物理定数、製造方法の詳細が確認できます。
https://kotobank.jp/word/%E8%87%AD%E5%8C%96%E9%8A%80-1383

【強力除菌消臭剤 ゲルタイプ 200g】マイガーディー 空間除菌 銀 亜鉛 金属イオン 酸化チタン 光触媒 細菌 ウイルス 無香料 塩素無 ノンアルコール 不燃 天然素材 香害 カビ Pm2.5 花粉不活化 化学物質過敏症 アトピー 送迎車 トイレ 赤ちゃん 防災対策 高評価 ジェル 日本製