電気分解電離違い
電気分解の基本的な仕組み
電気分解とは、電解質の溶液に電極を差し込み電流を流すことで、電極と溶液の間で酸化還元反応を起こし、電解質が分解される現象を指します。この反応では、外部から電気エネルギーを与えることで、通常は安定している水分子のような物質を強制的に分解することができます。電池で起こる酸化還元反応とは異なり、電気分解は不可逆反応であることが特徴です。
参考)電気分解とは?電気分解を理解して定期テスト10点アップ|高校…
電気分解では、2つの電極のうち電源のプラス極に接続された方を陽極、マイナス極に接続された方を陰極と呼びます。陽極では酸化反応が起こり、電子が奪われます。一方、陰極では還元反応が起こり、電子が与えられます。この仕組みにより、塩化銅水溶液の電気分解では陰極に単体の銅が析出し、陽極では気体の塩素が発生するのです。
参考)電気分解(原理・反応式・電池との関係など)
電気分解の装置は主に電極、電源、電解槽の3つで構成されています。電解液には水溶液中で電離する物質が使用され、塩化ナトリウムや水酸化ナトリウム、硫酸塩などが代表的な例として挙げられます。電流を流すと、陰イオンは陽極に引き寄せられて電子を放出し、陽イオンは陰極に引き寄せられて電子を受け取る仕組みになっています。
参考)【中学理科・復習】水酸化ナトリウム水溶液の電気分解とは?
電離の原理とイオン化
電離とは、物質が水に溶けて陽イオンと陰イオンに分かれる現象のことです。この現象は電気分解とは異なり、電流を流さなくても自然に起こります。水に溶けて電離する物質を電解質と呼び、電離しない物質を非電解質と呼びます。
参考)電気分解と電離の違いって何ですか? - 電離とはイオン化する…
塩化ナトリウムを例にとると、この物質は水に溶けるとナトリウムイオン(Na⁺)と塩化物イオン(Cl⁻)に分かれます。これはナトリウム原子が最外殻の電子を1個失い、塩素原子が電子を1個獲得することで、両方の原子がより安定な状態になるためです。水分子には+や-の電気を帯びている部分があり、この性質が電離を引き起こす重要な要因となっています。
参考)【中3理科】「電解質とイオン」(練習編)
youtube
電解質の水溶液は電流を通すという性質があります。これは水溶液中にイオンが存在し、そのイオンが電荷を運ぶことができるためです。一方、砂糖やエタノールなどの非電解質は水に溶けても電離せず、その水溶液は電気を通しません。イオン結合の逆を考えれば電離の仕組みが理解しやすくなります。
参考)中3化学【電離・電解質】
電気分解と電離の違いを化学反応式で理解
電気分解と電離の最大の違いは、化学変化が起こるかどうかという点にあります。電離は物質が水に溶けてイオンに分かれる現象であり、化学反応式で表すと塩化ナトリウムの場合「NaCl → Na⁺ + Cl⁻」となります。これは単にイオン結合が切れてイオンがバラバラになるだけで、新しい物質は生成されません。
一方、電気分解では実際に化学変化が起こります。塩酸の電気分解を例にとると、化学反応式は「2HCl → H₂ + Cl₂」となり、塩酸が水素ガスと塩素ガスという全く別の物質に分解されます。この違いは非常に重要で、電離と電気分解の式は別物として理解する必要があります。youtube
参考)塩酸の電気分解
電気分解においては、水溶液中で既に電離している状態のイオンを利用します。例えば塩化銅水溶液の電気分解では、まず塩化銅が電離して銅イオンと塩化物イオンになり、その後電気分解により銅イオンは陰極で還元されて金属銅になり、塩化物イオンは陽極で酸化されて塩素ガスになります。つまり電気分解には電離が前提として必要であり、両者は段階的な関係にあるのです。
参考)水溶液とイオン、電気分解(ざっくり)|教科の学習
電気分解の陶器製造との意外な関係
陶器や磁器の製造において、電気分解の原理が直接的に応用されているわけではありませんが、イオン化や電解質の概念は釉薬の化学的性質を理解する上で重要な役割を果たしています。陶磁器は「土」と「釉薬」の2種類で成り立っており、焼成時には複雑な化学反応が起こります。
参考)https://ceramicvalley.jp/valley/wp-content/uploads/2020/11/201124_%E3%82%AF%E3%83%AC%E3%82%A4%E3%82%B5%E3%83%9F%E3%83%83%E3%83%88%E7%AC%AC2%E9%83%A8.pdf
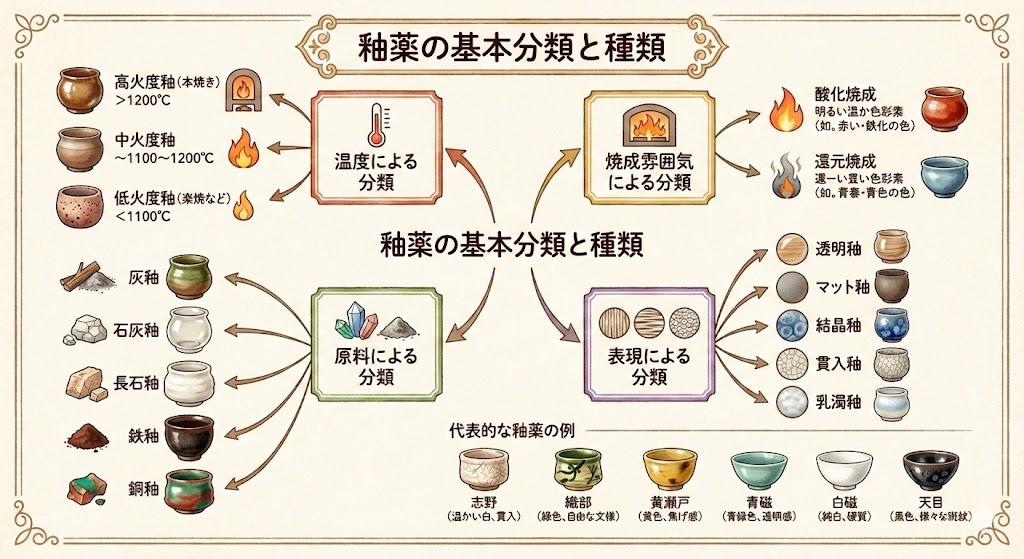
釉薬の成分には長石、珪石、粘土などが含まれており、焼成過程では1,200~1,300℃の高温で各成分が熔融して素地と固着します。この際、釉薬中の金属イオンが移動したり結合したりする過程は、イオンの性質と深く関わっています。例えば鉄釉という鉄分を含む釉薬では、鉄イオンの状態によって色調が変化します。
参考)http://igloss.web.fc2.com/cray/firing.htm
電気窯を使用した陶器の焼成では、正確な温度管理が可能になり、釉薬の化学反応をコントロールしやすくなっています。また、陶器の素地と釉薬の熱膨張係数の違いは、貫入(釉薬のヒビ)やシバリング(釉薬と生地の割れ)といった現象を引き起こすことがあり、これらは材料の化学的・物理的性質の理解なしには制御できません。近年では、電気化学的な手法を用いた新しい釉薬の開発や、廃棄カキ殻を釉薬として利用する研究なども進められており、イオン化学の知識が陶芸の分野でも活用されています。
参考)錫釉 - Wikipedia
電離と電気分解の日常生活での応用例
電離と電気分解は、私たちの日常生活の様々な場面で重要な役割を果たしています。電離は、食塩を水に溶かして料理をする際にも起こっており、溶解した塩化ナトリウムがナトリウムイオンと塩化物イオンに分かれることで、味を感じることができます。スポーツドリンクに含まれる電解質も、体内で電離してイオンとなり、神経伝達や筋肉の収縮に必要な電気信号を伝える役割を担っています。
参考)電離(イオン化) href="https://www.rerf.or.jp/glossary/ionizati/" target="_blank">https://www.rerf.or.jp/glossary/ionizati/amp;#8211; 公益財団法人 放射線影響研…
電気分解の応用例としては、水の電気分解による水素と酸素の生成が挙げられます。これは再生可能エネルギーを利用した水素燃料の製造に活用されており、クリーンエネルギー社会の実現に向けて注目されています。また、電気分解強酸性水は農業分野で病害防除に利用されており、キュウリうどんこ病などの作物病害を抑制する効果が確認されています。
参考)https://onlinelibrary.wiley.com/doi/pdfdirect/10.1002/aenm.202002453
身近な電池も電離と電気分解の原理を応用した装置です。乾電池では電解質が電離してイオンとなり、そのイオンの移動によって電流が流れます。一方、リチウムイオン二次電池では充電時に電気分解の原理で化学エネルギーを蓄積し、放電時にその逆反応で電気を取り出すことができます。さらに、電気分解を利用した水処理技術では、汚染物質を分解・除去することが可能で、環境保全にも貢献しています。
参考)https://jelectrochem.xmu.edu.cn/cgi/viewcontent.cgi?article=2136amp;context=journal
陶器や食器の表面に施される釉薬の化学的性質も、イオン化学と密接に関係しており、美しい色合いや光沢は金属イオンの化学反応によって生み出されています。このように、電離と電気分解の知識は、科学の基礎として様々な分野で実用化されているのです。
参考)瀬戸窯業試験場|研究成果|研究報告書

YukiRinKo 耐熱ガラス急須500ml 茶葉とお湯を分離 日本風シンプル 木製ハンドル付き 分解可能 電気陶磁器コンロ対応 家庭用 透明 グレー